Баланс бактерий кишечника играет важную роль в поддержании здоровья всего организма, а нарушение состава микробиоты связано с развитием многих заболеваний от депрессии до рассеянного склероза. Поэтому во всем мире проводятся различные исследования, позволяющие лучше понять взаимодействия микроорганизмов в микробиоте и возможность регуляции состава микробиоты для предотвращения развития болезней человека.
Ученые уже давно стараются найти способ для создания условий стабильности микробиоты. В новом исследовании определены ключевые факторы, которые позволяют полезным бактериям колонизировать те или иные участки кишечника.
Изначально ученые из Университета Корнеги стремились понять, как каждый бактериальный вид находит нужное место в желудочно-кишечном тракте для выполнения своих задач, а также каким образом минимизируются риски колонизации кишечника патогенными штаммами.
Команда исследователей под руководством Уилла Ладингтона из Карнеги-Смитсоновского института выявила гены, которые позволяют полезным видам бактерий колонизировать определённые участки желудочно-кишечного тракта. Их работа, опубликованная недавно в журнале Science, может кардинально изменить наше представление о том, как определяется состав микробиоты кишечника, и открыть двери для управлении им.
Микробиота кишечника — это экосистема, состоящая из сотен или тысяч видов микроорганизмов, которые живут в организме человека и влияют на наше здоровье, фертильность и даже продолжительность жизни. Эти популяции могут способствовать пищеварению, формировать иммунный ответ и помогать бороться с патогенами, а также выполнять другие функции, о чем можно прочитать в этой статье.
Однако микробиом неоднороден по всему кишечнику. Успешная колонизация каждого отдела желудочно-кишечного тракта различными популяциями микроорганизмов зависит от множества факторов, таких как потребность бактерий в питательных веществах, местный уровень кислотности и содержание растворённого кислорода, конкуренция с другими штаммами бактерий и выживаемость в суровых условиях, включая желудочную кислоту, соли желчных кислот и клетки иммунной системы.
Каждому виду необходимо попасть в нужное место, где он сможет процветать и способствовать здоровью хозяина. Исследователи пытались выяснить, как каждый вид бактерий попадает в нужное место и как свести к минимуму колонизацию вредными или неидеальными видами.
Представьте себе зарегистрированный багаж, перемещающийся по системе конвейерных лент за кулисами в оживленном городском аэропорту. Система обработки багажа может показаться неорганизованной и хаотичной, но большинство сумок доставляются в самолет туда, где им положено быть. И существуют процессы для исправления любой ошибочной сортировки, которая происходит со временем.
Точно так же в кишечнике полезные бактерии должны попасть в тот регион, где они смогут успешно создать колонию. Успешная колонизация зависит от белков клеточных стенок бактерий, называемых адгезинами. Как вы можете догадаться из их названия, они могут прилипать к множеству различных поверхностей в организме. Но обычно они связываются неспецифически, что означает, что они могут одинаково быстро прикрепляться к любой ткани.
Так как же виды симбиотического микробиома попадают туда, куда им нужно?
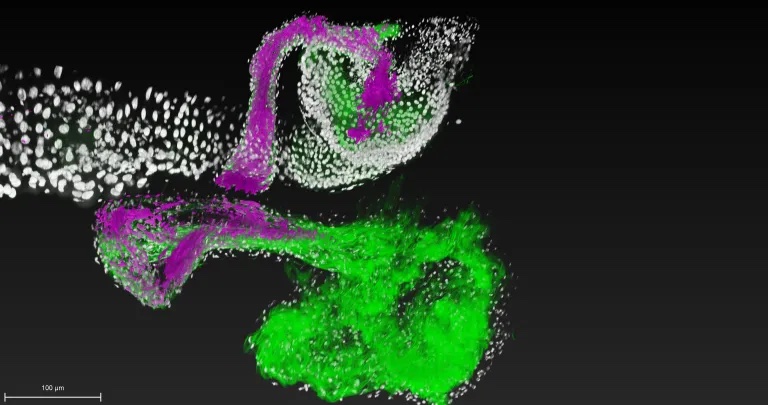
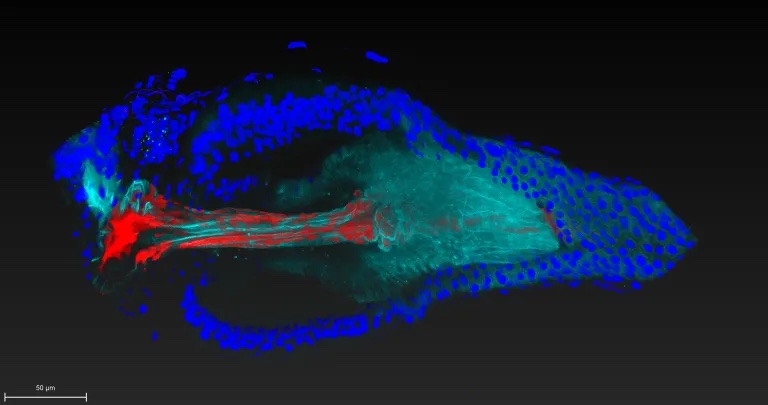
Чтобы разгадать эту загадку, ученые разработали технологию, которая позволила им наблюдать за тем, как одна бактериальная клетка вида Lactiplantibacillus plantarum в реальном времени колонизирует свою нишу в кишечнике плодовой мушки. Результат виден на фото.
Ученые обнаружили, что L. plantarum, выделенный из кишечника диких плодовых мушек, способен стабильно прикрепляться к тканям хозяина, в то время как L. plantarum, выделенный из организма человека и других источников, образует лишь временные связи.
Обладая этой информацией, исследователи решили определить генетическую основу этого сверхприспособления. Благодаря усердной и кропотливой работе они смогли выявить набор генов, отвечающих за симбиотическую колонизацию кишечника в пределах ниши. Это открывает возможности для создания пробиотиков, оптимизированных для заселения конкретных ниш в кишечнике человека.
Ранее в другом исследовании ученые пришли к выводу, что микробиота кишечника формируется нашими знакомыми и друзьями. Это открытие полностью изменило представление о факторах риска многих заболеваний, которые тесно связны с балансом бактерий кишечника.
Ученые провели уникальный эксперимент с жителями удаленных регионов Гондураса и пришли к выводу, что социальное взаимодействие непосредственно влияет на состав бактерий кишечника человека. Оказалось, что не только супруги и близкие друзья формируют микробиоту — влияние имеют даже знакомые и друзья друзей. Открытие полностью меняет представление ученых о факторах риска многих заболеваний, которые тесно связны с балансом бактерий кишечника.
Бактерии кишечника могут быть источником нейродегенерации, депрессии, аутоиммунных и других заболеваний. Многие исследования подтверждают эту связь, поэтому ученые стремятся понять механизмы формирования микробиоты. Ранее ученые из Стэнфордского университета обнаружили, что семья, друзья и все социальные контакты на протяжении жизни человека влияют на состав его микробиоты.
Новый эксперимент еще более информативен, поскольку авторы отправились в отдаленные регионы Гондураса — в 18 фактически изолированных деревень, где люди подвергаются минимальному воздействию обработанных пищевых продуктов и антибиотиков, которые могут изменить состав микробиоты. Выводы опубликованы на сайте Nature.
Оказалось, что проживающие в одном доме люди разделяют до 14% штаммов бактерий. Для друзей, с которыми люди часто проводят время, показатель составил 10%. При этом совпадение с другими жителями деревни (друзья друзей) было на уровне 4% — это намного больше, чем предполагалось.
Такие заболевания, как гипертония, депрессия и другие связаны с составом бактерий кишечника, о чем можно почитать здесь. Это означает, что они могут передаваться от человека к человеку через микробиоту, о чем можно почитать в этой статье. Это объясняет частое наличие «семейных» случаев патологии в нескольких поколениях семьи, ранее считавшихся наследственными или связанными с особенностями местной экологии. Оказалось, что в подавляющем количестве случаев это связано с носительством схожей микробиоты кишечника близко общающихся между собой людьми. Между тем ученые не рекомендуют избегать социальных контактов из-за страха «подхватить микробиоту» других людей. Социализация несет множество преимуществ, которые жизненно важны для психического здоровья.
Антибиотики могут легко справиться с инфекциями. Но как они влияют на сложные экосистемы дружественных бактерий, составляющих наш микробиом?
В новой работе, проведённой под руководством Людингтона и К.С. Хуана из Стэнфордского университета, учёные попытались ответить на этот сложный вопрос и обнаружили новую форму устойчивости к антибиотикам. Их результаты, имеющие важное значение для здравоохранения, опубликованы в eLife.
«Мы обнаружили, что взаимодействие между видами в экосистеме микробиома кишечника влияет на эффективность антибиотиков в уничтожении отдельных видов в этом сообществе, а также на метаболизм всего сообщества», — сказал Хуан.
Исследователи продемонстрировали, что когда бактерия Lactobacillus из микробиома плодовой мушки, которая также содержится в йогурте, выращивается вместе с бактерией Acetobacter, вырабатывающей уксус, она менее восприимчива к антибиотикам.
Это недавно обнаруженное явление, называемое устойчивостью к антибиотикам. Оно означает, что клетки, находящиеся вместе, погибают гораздо медленнее, чем если бы они были по отдельности. Устойчивость может быть опасной, потому что эта задержка повышает риск развития полной резистентности (невосприимчивости) к антибиотику.
Оказывается, ацетабактерии потребляют молочную кислоту, которая выделяется в качестве побочного продукта соседними лактобактериями, обеспечивая преимущество в выживаемости для обоих видов. Именно это происходит при ферментации и квашении, о чем можно почитать здесь и здесь. Поэтому квашенные овощи и комбуча (чайный гриб) показывают хороший результат при использовании их в качестве пробиотиков для заселения кишечника нормальной микробиотой.
Это может помочь скорректировать питание или образ жизни, чтобы предотвратить развитие легких проблем в серьезные заболевания. Понимание взаимодействий микроорганизмов в микробиоте и определение источников заселения микробиоты «правильными» видами бактерий могут дать людям возможность самостоятельно управлять своим здоровьем.
